کلید واژه ها
اصل لوشاتلیه
الیگومر
تبادل استری
برای ساخت پلیاستر با دو ترکیب شروع میکنیم. اگر شما صفحه مربوط به پلیاستر را خوانده باشید میدانید که این دو ترکیب اتیلنگلیکول و دیمتیلترفتالات هستند. اگر میخواهید این دو مولکول را به صورت سه بعدی ببنید اینجا کلیک کنید.
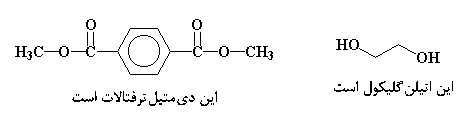
میدانیم که دیمتیلترفتالات یک استر و اتیلنگلیکول یک الکل است. وقتی که الکلها و استرها به هم میرسند، واکنشی تحت عنوان تبادل استری صورت میگیرد.
به گروههای متوکسی (بارنگ قرمز) روی دیمتیلترفتالات و گروههای هیدورکسیاتوکسی (با رنگ آبی) روی اتیلنگلیکول، توجه کنید. این دو گروه میخواهند جاهایشان را با هم عوض کنند. گروه هیدروکسیاتوکسی میخواهد سر از مولکول استر دربیاورد، یعنی جایی که قبلاً گروه متوکسی قرار داشت. و گروه متوکسی هم میخواهد به یک هیدروژن متصل شود، جایی که پیش از این گروه هیدروکسیاتوکسی قرار داشت.
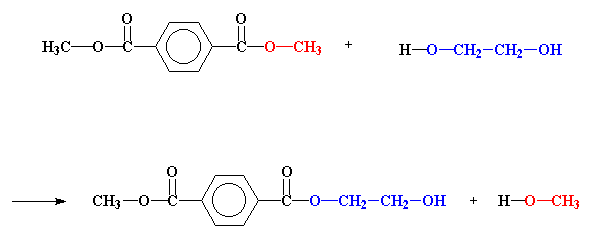
همه ی آنچه که گفتیم، در اولین مرحله از ساخت پلی استر اتفاق می افتد. بیایید ببینیم اینها چگونه انجام می شوند.
به دیمتیلترفتالات، و به خصوص کربن کربونیل آن توجه کنید. دقت کنید که با یک باند دوگانه به اکسیژن متصل است. اکسیژن بسیار الکترونگاتیوتر از کربن است. بنابراین الکترونها را از کربن به سمت خود میکشد و این باعث میشود که مقداری بار جزئی مثبت بر روی کربن به جا بماند. و این یعنی میتواند به راحتی از جانب یک جفت الکترون مورد حمله قرار بگیرد.
حالا این جفت الکترون دقیقاً از کجا میآید؟
وقتی یک الکل مانند اتیلنگلیکول در آن اطراف باشد، جفت الکترونهای آزاد اتمهای اکسیژن الکل این کار را به خوبی انجام میدهند. آنها درست مانند شکل زیر به کربن حمله میکنند.
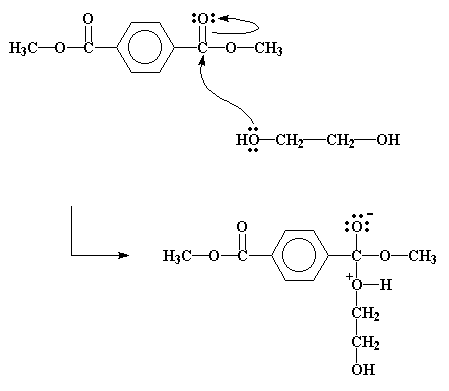
در اینجا یک جفت الکترون از باند دوگانه کربن-اکسیژن به بیرون از باند و به روی اکسیژن کربونیل به زور هل داده میشود، و بدین ترتیب یک بار منفی به اکسیژن میرسد. ضمناً اکسیژن الکل نیز دارای یک بار مثبت میشود. این ترکیب واسطه موجب یک نوآرایی در الکترونها میشود که با فلش در شکل بالا نشان داده شده است. نتیجهی همهی این نوآراییها این است که گروه هیدروکسیاتیل از اتیلنگلیکول به استر میچسبد و گروه متیل از استر به شکل مولکول متانول به بیرون پرتاب میشود.
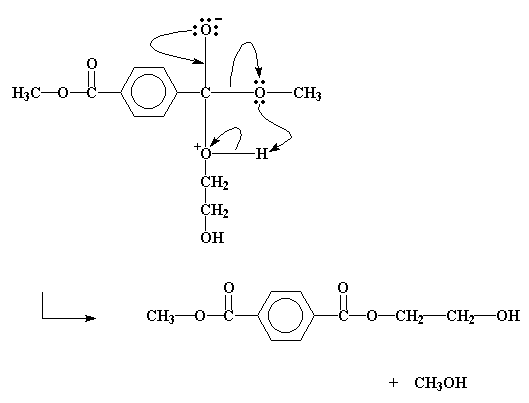
و بالاخره گروه هیدروکسیاتیل و گروه متیل از جابه جا شدن دست بر میدارند.
این متانول یک محصول فرعی است که ما نمیخواهیم در آن اطراف باشد. اگر ما این واکنش را در دمایی که به اندازه کافی بالا باشد انجام دهیم، متانول میجوشد و از محیط واکنش بیرون میرود. این کار نه تنها باعث خلاص شدن از متانول میشود، بلکه بیرون کردن محصول جانبی، واکنش تبادل استری را به سمت تبدیل بالاتر میبرد. اصل لوشاتلیه را به یاد میآورید؟
اگر میخواهید فیلمی از واکنش کامل تبادل استری ببنید، اینجا کلیک کنید.
همین واکنش در سمت دیگر ترفتالات روی میدهد و به ما بیس(۲- هیدروکسیاتیل)ترفتالات را میدهد.
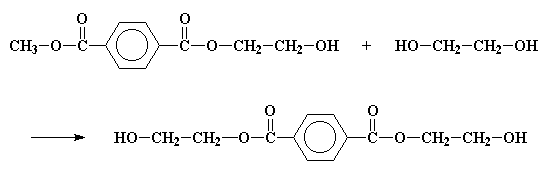
اگر میخواهید بیس(۲- هیدروکسیاتیل)ترفتالات را به صورت سه بعدی ببنید، اینجا کلیک کنید.
بیس(۲- هیدروکسیاتیل)ترفتالات به دست آمده، واکنشهای بیشتری انجام میدهد. اما این واکنشها را به راحتی میتوان دنبال کرد، چون همهی آنها مشابه آنچه که دیدید، واکنش تبادل استری هستند. این مولکول یک الکل و یک استر است. بنابراین میتواند همان طور که در شکل زیر نشان داده شده با خودش تبادل استری کند.
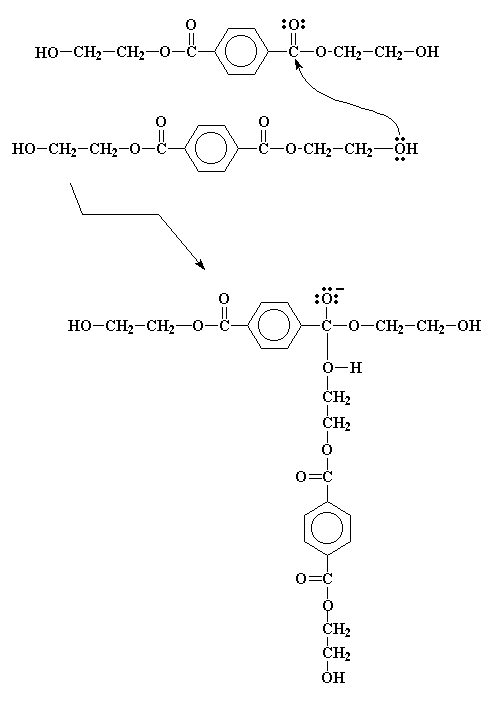
این واکنش یک ترکیب واسطه میسازد، مشابه آنچه پیش از این دیدیم، و بدون هیچ گونه غافلگیری باز هم یک سری بازآراییهای الکترونی روی میدهد تا محصولی که در زیر میبینیم تشکیل شود.
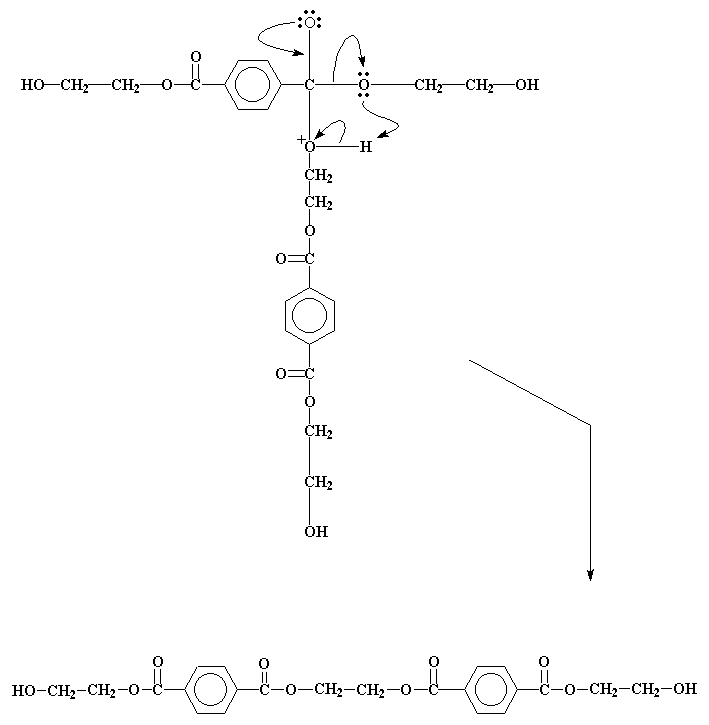
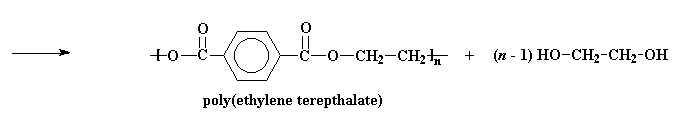
این محصول میتواند باز هم واکنش دهد، درست همان طور که بیس(۲- هیدروکسیاتیل)ترفتالات این کار را کرد. و وقتی این اتفاق بیفتد این مولکول بزرگ و بزرگ تر می شود تا جایی که به وزن مولکولی بالای PET می رسیم.
 my
my
عالی بود
ممنون
خیلی خوب بود
برای شروع واکنش پلیمر شدن چه آغاز گری می تونه استفاده بشه؟
اگه بجای اتیلن گلیکول از پلیمری مانند نشاسته استفاده شود آیا کوپلیمر تشکیل می شود؟
یا اگه بجای دی متیل ترفتالات از یک دی کربوکسیلیک ( تارتاریک اسید) استفاده بشه آیا پلیمر حاصل می شود؟
لطفا پاسخ دهید
سلام ۱- واکنش پلیمریزاسیون کندانسیونی نیاز به آغازگر ندارد و صرفا با دما واکنش جلو میره
۲- می تونید برسی کنید توی مقالات ولی من دیدم که نشاسته رو با آکریلاتی کردن کو پلیمر کرده اون قطعا راحت تر خواهد بود
۳ – بله اگر اسید دو عاملی باشد پلیمر میشه مرسوم ترفتالیک اسید هست
عااااااالییییی بود ممنون
عالی بود مرسی خیلی استفاده کردم