پلیمریزاسیون زیگلر-ناتا یکی از روشهای پلیمریزاسیون وینیلی است. این فرآیند، از آنجایی که ساخت پلیمرهایی با تاکتیسیتهی مشخص را برای ما میسر میسازد، اهمیت زیادی دارد. این روش توسط دو دانشمند کشف شد و فکر میکنم همهی ما بتوانیم نام آنها را حدس بزنیم. زیگلر-ناتا بسیار مفید است، زیرا میتواند پلیمرهایی را بسازد که با هیچ روش دیگر قابل ساخت نیستند، مانند پلیاتیلن خطی بدون شاخه و پلیپروپیلن ایزوتاکتیک. پلیمریزاسیون وینیلی رادیکال آزاد فقط میتواند پلیاتیلن شاخهدار تولید کند و پلیپروپیلن اصلاً با روش پلیمریزاسیون رادیکال آزاد، ساخته نمی شود. لذا این واکنش، یعنی زیگلر-ناتا، واکنش پلیمریزاسیون بسیار مهمی است.
برقراری شرایط مناسب برای انجام پلیمریزاسیون زیگلر-ناتا، غالباً به جادو شبیه تر است تا به علم. با این حال ما هم کمی درباره ی آن اطلاعات داریم. می دانیم که این روش شامل کاتالیزور های فلزات واسطه نظیر ![]() است. همچنین می دانیم که کوکاتالیزور هایی هم وجود دارند که معمولاً مبتنی بر فلزات گروه
است. همچنین می دانیم که کوکاتالیزور هایی هم وجود دارند که معمولاً مبتنی بر فلزات گروه ![]() مثل آلومینیوم می باشند. اکثر اوقات، زوجِ کاتالیزور/کوکاتالیزور
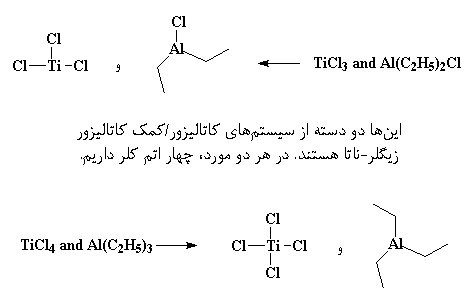
مثل آلومینیوم می باشند. اکثر اوقات، زوجِ کاتالیزور/کوکاتالیزور ![]() و
و ![]() ، یا
، یا ![]() و
و ![]() هستند.
هستند.
برای راحتی کار، ![]() و
و ![]() را در نظر می گیریم. دانستن برخی مطالب در مورد
را در نظر می گیریم. دانستن برخی مطالب در مورد ![]() به فهم چگونگی کار سیستم و تولید پلیمر توسط آن، کمک می کند.
به فهم چگونگی کار سیستم و تولید پلیمر توسط آن، کمک می کند. ![]() می تواند خودش را در چندین ساختار بلوری، منظم کند. ساختاری که ما بدان علاقمندیم،
می تواند خودش را در چندین ساختار بلوری، منظم کند. ساختاری که ما بدان علاقمندیم، ![]() است، با ساختاری شبیه به این:
است، با ساختاری شبیه به این:
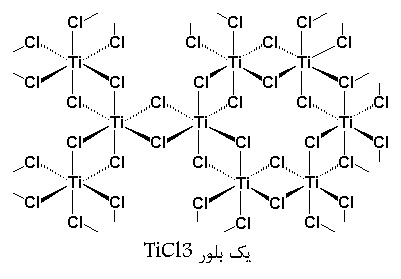
همان گونه که میببینیم، هر اتم تیتانیوم با ۶ اتم کلر مرتبط است و دارای شکل هندسی هشت وجهی میباشد. زمانی که تیتانیوم با شش اتم دیگر در رابطه است، بهترین حالت برای اتم تیتانیوم است. ولی همین مسئله اشکالاتی را هم برای اتمهای تیتانیوم در سطح بلور ایجاد میکند. در داخل بلور، هر تیتانیوم با شش اتم کلر احاطه شده است، ولی در سطح بلور، یک اتم تیتانیوم در یک طرف با ۵ اتم کلر ارتباط دارد و در سمت دیگر با فضای خالی مرتبط است.
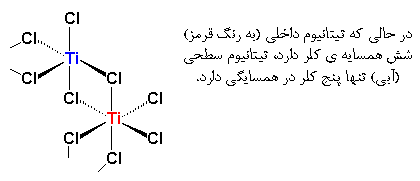
این امر باعث می شود که تیتانیوم دچار کمبود یک کلر شود. می دانید که تیتانیوم یک فلز واسطه است، و می دانیم که این عناصر، شش اوربیتال خالی (یعنی یک اوربیتال ![]() و پنج اوربیتال
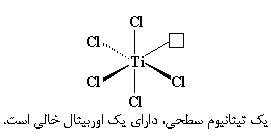
و پنج اوربیتال ![]() ) در خارجی ترین لایه ی الکترونی خود دارند. برای راضی بودن، تیتانیوم باید با تعداد کافی از اتم ها ارتباط یابد، تا در هر اوربیتال خود، دو الکترون قرار دهد. اتم تیتانیوم روی سطح بلور آن قدر اتم در همسایگی خود دارد که بتواند تنها ۵ اوربیتال از ۶ اوربیتال خود را پُر کند و یک اوربیتال خالی می ماند، که در شکل زیر با مربع نشان داده شده است.
) در خارجی ترین لایه ی الکترونی خود دارند. برای راضی بودن، تیتانیوم باید با تعداد کافی از اتم ها ارتباط یابد، تا در هر اوربیتال خود، دو الکترون قرار دهد. اتم تیتانیوم روی سطح بلور آن قدر اتم در همسایگی خود دارد که بتواند تنها ۵ اوربیتال از ۶ اوربیتال خود را پُر کند و یک اوربیتال خالی می ماند، که در شکل زیر با مربع نشان داده شده است.
البته این وضعیت نمی تواند ادامه یابد. تیتانیوم مذکور، می خواهد اوربیتال های خود را پُر کند. اما ابتدا، ![]() وارد صحنه می شود. این مولکول، یکی از گروه های اتیل خود را به تیتانیوم می دهد، اما در حین فرآیند، یکی از کلرها را بیرون می کند. با این حال، هنوز یک اوربیتال خالی داریم که به زودی درباره ی آن صحبت خواهیم کرد.
وارد صحنه می شود. این مولکول، یکی از گروه های اتیل خود را به تیتانیوم می دهد، اما در حین فرآیند، یکی از کلرها را بیرون می کند. با این حال، هنوز یک اوربیتال خالی داریم که به زودی درباره ی آن صحبت خواهیم کرد. 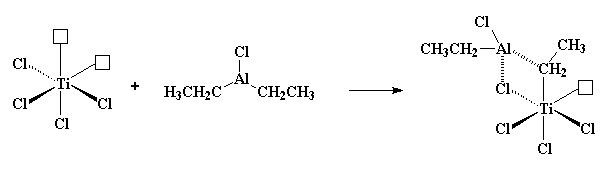
همان گونه که در این شکل می بینید، آلومینیوم همچنان با اتم کربن ![]() از گروه اتیل در ارتباط باقی می ماند، هر چند با آن پیوند کوالانسی برقرار نمی کند. این
از گروه اتیل در ارتباط باقی می ماند، هر چند با آن پیوند کوالانسی برقرار نمی کند. این![]() همان گروهی است که آلومینیوم در اختیار تیتانیوم قرار داده است. علاوه بر این، آلومینیوم خودش را با یکی از اتم های کلر متصل به تیتانیوم نیز مرتبط میکند. اما تیتانیوم هنوز هم یک اوربیتال خالی دارد که باید پُر شود.
همان گروهی است که آلومینیوم در اختیار تیتانیوم قرار داده است. علاوه بر این، آلومینیوم خودش را با یکی از اتم های کلر متصل به تیتانیوم نیز مرتبط میکند. اما تیتانیوم هنوز هم یک اوربیتال خالی دارد که باید پُر شود.
بعد از این مرحله یک مونومر وینیلی مثل پروپیلن وارد می شود. دو الکترون در سیستم π یک پیوند دوگانه ی کربن-کربن وجود دارد. این الکترون ها می توانند برای پر کردن اوربیتال خالی تیتانیوم استفاده شوند. ما می گوییم که پروپیلن و تیتانیوم یک کمپلکس تشکیل می دهند و آن را به این صورت نمایش می دهیم:
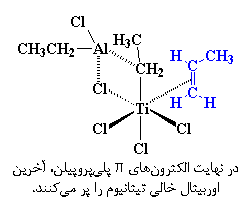
با این حال، کمپلکس شدن، فرآیند نسبتاً پیچیدهای است، و به سادگی آنچه این شکل نشان میدهد، نیست. اگر از قبل میدانید که فرآیند کمپلکس شدن به چه ترتیبی است، لازم نیست به سراغ بخش بعدی بروید، و میتوانید مستقیماً به بخش پلیمریزاسیون وارد شوید. ولی اگر این طور نیست، مطالعهی این صفحه را به همین ترتیب ادامه بدهید تا بفهمید که کمپلکس شدن چگونه عمل میکند.
درباره کمپلکس شدن آلکن-فلز بیاموزید
ورود مستقیم به پلیمریزاسیون
کمپلکسهای آلکن-فلز
اکنون یک مونومر وینیلی، مثلاً یک مولکول پروپیلن را در نظر بگیرید. تیتانیوم قصد دارد از حضور این مونومر استفاده کند. برای فهمیدن دلیل این امر، بیایید به مونومر وینیلی، مخصوصاً به پیوند دوگانه ی آن، نگاهی بیاندازیم. یک پیوند دوگانه ی کربن-کربن، از یک پیوند σ و یک پیوند π تشکیل شده است. قصد داریم نگاهی دقیق تر به پیوند π داشته باشیم.
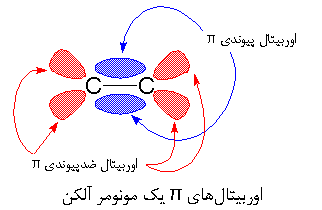
اگر نگاهی به شکل بالا بیندازید، خواهید دید که پیوند π، شامل دو اوربیتال π است؛ یکی اوربیتال پیوندی π (به رنگ آبی) و دیگری اوربیتال ضد پیوندی π (به رنگ قرمز). اوربیتال پیوندی، دو لُب دارد که بین اتمهای کربن هستند، و اوربیتال ضد پیوندی، دارای چهار لب است که به سمت خارج از اتمهای کربن قرار گرفتهاند. معمولاً زوج الکترونها داخل اوربیتال پیوندی میمانند. اوربیتال ضد پیوندی از نظر انرژی در سطح بالایی است، و بدین ترتیب در شرایط عادی خالی میماند..
دوباره به تیتانیوم نگاه کنیم. این شکل تیتانیوم و دو اوربیتال d آن را نشان می دهد. اکنون برای اطمینان، یادآوری می کنیم که تیتانیوم بیش از دو اوربیتال d دارد که ما برای راحتی و وضوح، دو تا از آنها را نشان می دهیم.

یکی از اوربیتال های تیتانیوم نشان داده شده، همان اوربیتال خالی است. این اوربیتال از لب های سبزرنگ ساخته شده است. لبهای صورتی یکی از اوربیتالهای پر هستند. اوربیتال خالی به دنبال یک زوج الکترون می گردد و می داند آن را در کجا جستجو کند. این اوربیتال میداند که اوربیتال پیوندی π آلکن، زوج الکترون دارد که می تواند آن را به اشتراک گذارد. بنابراین اوربیتال پیوندی π آلکن و اوربیتال d تیتانیوم به هم نزدیک می شوند و یک زوج الکترونی به اشتراک می گذارند.
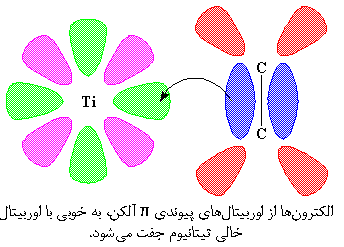
اما به محض اینکه این دو به هم می رسند، اوربیتال d دیگر هم، بسیار به اوربیتال خالی ضد پیوندی π نزدیک می شود. بنابراین اوربیتال d و اوربیتال ضد پیوندی π نیز یک زوج الکترون به اشتراک می گذارند.
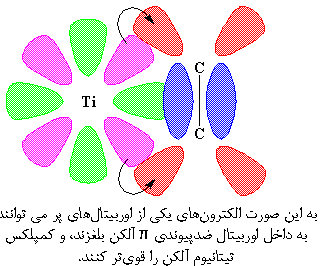
این اشتراک اضافی الکترونها، کمپلکس را مقاومتر میکند. کمپلکس شدن بین آلکن و تیتانیوم، همه چیز را برای مرحلهی بعدی که پلیمریزاسیون است، آماده میکند
پلیمریزاسیون
بخش نخست: پلیمریزاسیون ایزوتاکتیک
ماهیت دقیق کمپلکس بین تیتانیوم و پروپیلن، پیچیده است. بنابراین به منظور ساده سازی، ما قصد داریم آن را همان طور که از اول رسم کردهایم، ساده رسم کنیم. مثل این:
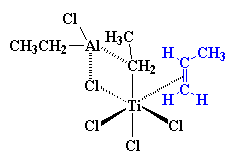
کمپلکس خوبی است و مشکل تیتانیوم را حل میکند (همان مشکل مربوط به نداشتن الکترون کافی برای پر کردن اوربیتالهای d). اما تیتانیوم نمیتواند به این صورت ادامه دهد. میدانید که کمپلکس قرار نیست برای همیشه به همین شکل باقی بماند؛ و یک جابجایی الکترونی در آستانهی انجام است. چندین زوج الکترون قصد دارند که تغییر موقعیت دهند. انتقال را میتوانید در شکل زیر ببینید:
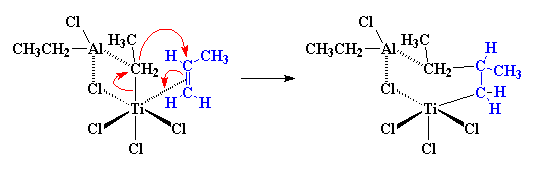
دقیقاً نمیدانیم که ابتدا کدام زوج منتقل می شود، اما فکر می کنیم اولین زوج، از پیوند π کربن-کربن که با تیتانیوم کمپلکس شده است، جا به جا می شوند. این زوج، منتقل می شود تا پیوند ساده ی کربن-تیتانیوم را تشکیل دهد. سپس الکترون ها از پیوند بین تیتانیوم و کربن گروه اتیل، که تیتانیوم آن را از ![]() گرفته بود، منتقل می شود. این زوج الکترون قصد دارد به منظور ایجاد یک پیوند بین گروه اتیل و کربن متیل دار مونومر پروپیلن، جابجا شود. بیان آن با کلمات کمی سخت است، اما ما نهایتاً به ساختاری می رسیم که شما در سمت راست شکل بالا می بینید.
گرفته بود، منتقل می شود. این زوج الکترون قصد دارد به منظور ایجاد یک پیوند بین گروه اتیل و کربن متیل دار مونومر پروپیلن، جابجا شود. بیان آن با کلمات کمی سخت است، اما ما نهایتاً به ساختاری می رسیم که شما در سمت راست شکل بالا می بینید.
آنچه را که در مرحله ی بعد اتفاق می افتد، مهاجرت می نامیم. علت وقوع این پدیده معلوم نیست. فقط می دانیم که اتفاق می افتد. اما اتم ها خودشان را نوآرایی می کنند تا ساختاری کمی متفاوت، مثل شکل زیر را تشکیل دهند:
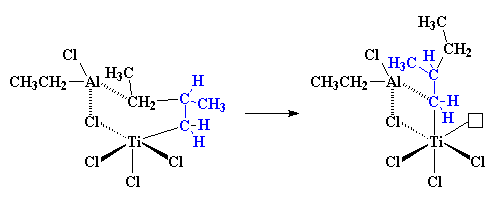
حال، همان طور که میبینید آلومینیوم با یکی از اتمهای کربن از مونومر پروپیلن کمپلکس شده است. باز هم ملاحظه می کنید که تیتانیوم دوباره به وضعیت آغازین خود باز گشته است، یعنی یک اوربیتال خالی دارد که باید آن را پر کند.
بنابراین هنگامی که یک مولکول دیگر پروپیلن وارد میشود، تمام فرآیند دوباره از اول شروع شده و نتیجهی نهایی چیزی شبیه این خواهد بود:
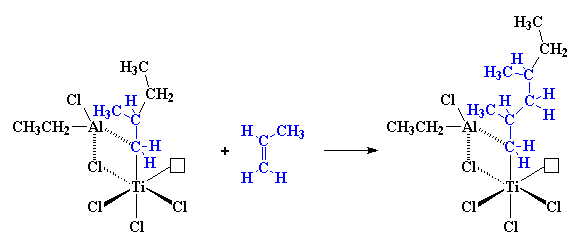
و البته، مولکولهای پروپیلنِ بیشتر و بیشتری واکنش داده و زنجیر ما مرتباً رشد میکند. اگر نگاهی به تصویر بیندازید، میبینید که همهی گروههای متیل پلیمر در حال رشد، در یک طرف زنجیر قرار دارند. با این مکانیسم، پلیپروپیلن ایزوتاکتیک به دست میآید. مولکول پروپیلن ورودی، فقط در صورتی میتواند واکنش دهد که در جهت درست قرار گرفته باشد، یعنی در جهتی که پلی پروپیلن ایزوتاکتیک تولید کند. ما علت این پدیده را نمیدانیم، ما فقط میدانیم که اتفاق میافتد.
اگر می خواهید فیلمی از پلیمریزاسیون زیگلر-ناتای ایزوتاکتیک ببینید، اینجا کلیک کنید.
بخش دوم: پلیمریزاسیون سیندیوتاکتیک
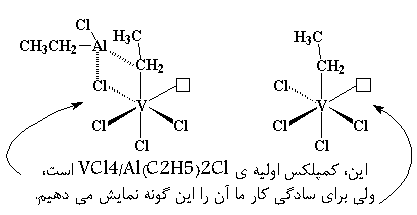
سیستم کاتالیزوریای که تا کنون بررسی کردهایم، پلیمرهای ایزوتاکتیک تولید میکند. اما سیستمهای دیگر میتوانند پلیمرهای سیندیوتاکتیک بدهند. سیستمی که ما قصد بررسی آن را داریم، به جای تیتانیوم بر پایهی وانادیوم است. این سیستم ![]() و شبیه تصویری است که در زیر و در سمت چپ میبینید، و با سیستم تیتانیوم که قبلاً آن را دیدهاید تفاوت چندانی ندارد. اما برای ساده کردن این بحث کوتاه، قصد داریم سیستم را به صورت تصویر سمت راست بکشیم.
و شبیه تصویری است که در زیر و در سمت چپ میبینید، و با سیستم تیتانیوم که قبلاً آن را دیدهاید تفاوت چندانی ندارد. اما برای ساده کردن این بحث کوتاه، قصد داریم سیستم را به صورت تصویر سمت راست بکشیم.
این کمپلکس، هنگامی که یک مولکول پروپیلن بر سر راه آن قرار میگیرد، کاملاً به شیوهی سیستم تیتانیومی عمل می کند: ابتدا پروپیلن با وانادیوم کمپلکس تشکیل میدهد، سپس الکترونها درست مثل قبل، جابه جا میشوند و پروپیلن بین فلز و گروه اتیل، مانند قبلی، قرار میگیرد.
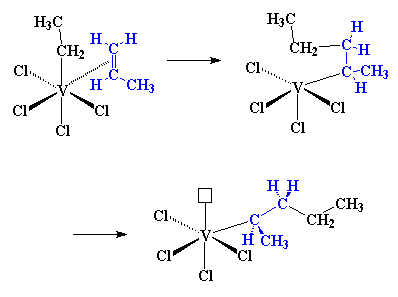
اما شما میتوانید تفاوت مهمی را هم در این تصویر ببینید. به یاد میآورید که در سیستم تیتانیومی، زنجیر پلیمری در حال رشد چگونه روی اتم تیتانیوم تغییر موقعیت میداد؟ ملاحظه میکنید که این امر در این جا اتفاق نمیافتد. پلیمر در حال رشد، تا زمانی که مولکول پروپیلن دیگری وارد نشده است، در موقعیت جدید خود میماند. مولکول پروپیلن دوم در حالی که زنجیر هنوز در موقعیت جدید خود قرار دارد، واکنش میدهد، درست مثل آن چه اینجا میبینید:
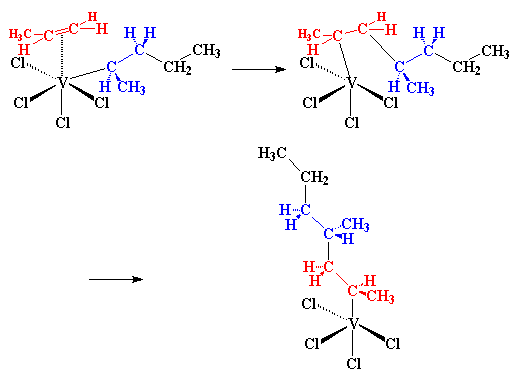
اما ملاحظه میکنید هنگامی که پروپیلن دوم به زنجیر اضافه شد، زنجیر دوباره موقعیتش را تغییر میدهد. زنجیر به موقعیتی باز میگردد که از آنجا شروع کرده بود. به گروههای متیل مونومر اول، به رنگ آبی، و مونومر دوم، به رنگ قرمز، نگاهی بیاندازید. توجه کنید که آنها در دو طرف مخالف زنجیر پلیمر قرار دارند. هنگامی که زنجیر پلیمر در حال رشد در یک موقعیت قرار دارد، مونومر پروپیلن تنها به صورتی میتواند اضافه شود که گروه متیل در طرف خاصی از زنجیر باشد. وقتی زنجیر در موقعیت دیگری باشد، پروپیلن تنها میتواند به صورتی اضافه شود که گروه متیل به طرف دیگر کشیده شود. علت دقیق این پدیده معلوم نیست. اما میدانیم، ازآنجایی که زنجیر پلیمر رشد کننده، موقعیتش را با اضافه شدن هر مونومر پروپیلن عوض میکند، سرانجام گروههای متیل به طور متناوب در طرفین زنجیر قرار میگیرند نتیجتاً یک پلیمر سیندیوتاکتیک حاصل میشود.
اگر میخواهید فیلمی دربارهی چگونگی انجام پلیمریزاسیون زیگلر-ناتای سیندیوتاکتیک ببینید، اینجا کلیک کنید.
محدودیتها
پلیمریزاسیون زیگلر-ناتا، روش مناسبی برای ساخت پلیمرهایی از مونومرهای هیدروکربنی مثل اتیلن و پروپیلن است. اما روی برخی از انواع دیگر مونومرها اثری ندارد. به عنوان مثال، نمیتوانیم پلی(وینیل کلراید) را با پلیمریزاسیون زیگلر-ناتا بسازیم. هنگامی که کاتالیزور و کمک کاتالیزور با هم جمع میشوند تا کمپلکس اولیه را بسازند، طی مراحل میانی واکنش، رادیکالهایی تولید میشوند که میتوانند پلیمریزاسیون رادیکال آزاد مونومر وینیل کلراید را شروع کنند. این روش برای آکریلاتها هم مناسب نیست، زیرا کاتالیزورهای زیگلر-ناتا اغلب پلیمریزاسیون وینیلی آنیونی را در این مونومرها شروع میکنند.
حرکت روبه جلو
برای زمانی طولانی، پلیمریزاسیون زیگلر-ناتا مفیدترین واکنش برای ساخت پلیمرهای دارای نظم فضایی دلخواه بود. اما اخیراً نوع جدیدی از پلیمریزاسیون ارائه شده است که آن هم از کمپلکسهای فلزی به عنوان شروعکننده استفاده میکند. این روش، پلیمریزاسیون کاتالیزوری متالوسن نامیده میشود و یک روش کاملاً جدید محسوب میشود، پس دربارهی آن مطالعه کنید.
 my
my
سلام خسته نباشید من از کجا پلی اتلین میتونم تهیه کنم
جناب حسن زاده . خیلی ممنونم بابت لطفی که داشتید برای گردآوری این مطلب
بسیار عالی . لطفا فیلمی در رابطه با این مطلب قرار دهید.
سلام خسته نباشید دمتون گرم بی نظیر بود…
خیلی خوب بود. سپاسگزارم
سلام. وقتتون بخیر. ممنون بخاطر مطالب مفیدتون.
ببخشید لطفا رفرنس این مطلب رو برام میفرستین. با تشکر فراوان
عمده مطالب این بخش ترجمه ای از پروژه آموزنده ماکروگالریا می باشد.
http://www.pslc.ws/macrog/index.htm
با سپاس
عالی بود توضیحات و تقریبا جامع
خیلی متشکرم عالی بود
کامل و واضح بود
ممنون عالی بود
عالی بود متشکرم
با سلام درخواست منابع متن گذاشته شده رادارم با تشکر
عمده مطالب این بخش ترجمه ای از پروژه آموزنده ماکروگالریا می باشد.