محققین در گذشته توانسته اند داروهای سرطانی را توسط نانوذرات تزریق کنند. اخیراً محققین دانشگاه هاروارد و MIT توانسته اند برای درمان بیماری های قلبی، ذراتی طراحی کنند که با چسبیدن به دیوارههای رگ، دارو را به آرامی آزاد کند.
ذراتی که nonaburrs یا نانوذرات خاردار خوانده میشوند، توسط تکههای پروتئینی کوچکی پوشیده میشوند که امکان چسبیدن به دیواره رگها را به آنها میدهد. پس از چسبیدن این ذرات به دیواره رگ، داروهایی مانند paclitaxel که از تقسیم سلولی و رشد بافت زخم جلوگیری میکند، آزاد میشوند.
پروفسور لانگر، یکی از این محقیقن می گوید: «این روش یکی از نمونههای جالب و شگفت انگیز کاربرد نانوتکنولوژی و هدف گیری سلولی است و من امیدوارم که این تکنولوژی بیشتر گسترش یابد».
آقای مارک دیویس، پروفسور رشته ی مهندسی شیمی در Caltech گفت: «این کار یک قدم نوید بخش در درمان بیماریهای قلبی و سایر بیماریها است و اگر آنها بتوانند این کار را بر روی بیماران با موفقیت انجام دهند در واقع فرصتهای بسیار زیادی را به وجود آورده اند.» البته آقای دیویس در این تحقیق شرکت نکرده است.
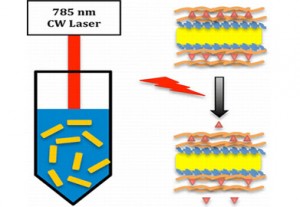
یکی از راههای معمول در درمان رگهای خونی آسیب دیده و مسدود شده، وارد کردن یک لوله نازک مجرا دار (استنت) است که رگ خونی را باز نگه میدارد و دارویی مانند paclitaxel تزریق میشود. محققین امیدوارند بتوانند در جایی مانند محل چند شاخه شدن رگ که استفاده از استنتها مناسب نیست، از این nanoburr های جدید برای درمان محل آسیب دیده استفاده کنند. Nanoburr ها به سمت بافت معینی بنام غشاءهای زیرین فرستاده میشوند. این بافت تنها در محلهایی که دیواره رگ آسیب دیده تشکیل می شود و با آسیب دیدن رگ، مانند یک آستر دیوارهی آن را میپوشاند. گروه تحقیقاتی برای ساخت نانو ذرات خود مجموعه ای از باندهای پپتیدی متوالی کوچک را بررسی کردند تا باندهایی که بیشترین تأثیر را بر روی ملکولهای روی سطح غشاءهای زیرین دارند پیدا کنند. آنها از یک آمینو اسید هفت تایی پر کاربرد بنام C11 برای پوشاندن لایه خارجی نانو ذره خود استفاده کردند.
هسته داخلی ذرات با قطر nm60 حامل دارو است که به زنجیر پلیمری بنام پلی لاکتیک اسید متصل شده است. لایه وسطی بین هسته ی داخلی و پوسته خارجی یک ماده چربی بنام سویبین لسیتین است که شامل پلیمری به نام پلی اتیلن گلیکول است. این پلیمر در جریان خونی رگ، از ذرات محافظت میکند.

دارو زمانی میتواند آزاد شود که از زنجیر پلیمری PLA (واقع در هسته ذره) جدا شود. این عمل به کندی و به تدریج توسط یک واکنش هیدرولیز استری انجام میشود. هر چه طول زنجیر بیشتر باشد، این فرآیند بیشتر طول میکشد. محققین توانستهاند زمان آزاد شدن دارو را با عوض کردن طول زنجیر کنترل کنند. آنها تاکنون توانستهاند در یک آزمایش کنترل شده سلولی، دارو را در مدت ۱۲ روز آزاد کنند.
Uday Kompella پروفسور داروسازی در دانشگاه Colorado می گوید: «ساختار nanoburrمیتواند تولید آنرا آسانتر کند، چرا که پپتیدهای هدف گیری شده به پوسته بیرونی چسبیدهاند و مستقیماً به هستهی داخلی که دارو را حمل میکند، متصل نیستند، که البته اینکار به یک سری واکنشهای شیمیایی پیچیده تری نیاز داشت. همچنین این طراحی احتمال شکافتن و ترکیدن ناگهانی را کاهش میدهد.»
یکی دیگر از مزیتهای nanoburrها این است که میتوانند در ورید در یک فاصله مکانی از بافت آسیب دیده تزریق شوند. محققین نشان دادهاند که nanoburrهای تزریق شده در نزدیکی بافت میتوانند به هدف خواسته شده یعنی همان دیوارهی رگ خونی آسیب دیده بچسبند.
Julliana Chan میگوید: به دلیل اینکه این ذرات میتوانند داروها را در یک دوره زمانی طولانیتر آزاد کنند و میتوانند به درون ورید تزریق شوند، دیگر لازم نیست که بیماران جراحیهای خطرناک را تحمل کنند.
این تیم اکنون بیشترین تأثیر دارو در معالجه و درمان بافتهای رگی آسیب دیده را در یک دوره زمان دو هفته ای بررسی میکنند. این ذرات همچنین میتواند در رساندن دارو به تومور نیز مفید باشد. دکتر امید فرخزاد میگوید: «این تکنولوژی میتواند کاربردهای بیشتری نیز داشته باشد به خصوص در بیماریهایی مثل سرطان و بیماریهایی که در آن آسیب رگهای خونی یا مسدود شدن آنها مشاهده میشود».
———————
 my
my