امولسیون این چنین تعریف میشود: «یک سوسپانسیون کلوییدی پایدار، مانند شیر، مرکب از مایعی امتزاجناپذیر که توسط مادهای به نام امولسیفایر، در مایع دیگری پراکنده و نگه داشته شده است.»
به منظور درک پلیمریزاسیون امولسیونی و نیز امولسیفایر، ابتدا باید چگونگی عملکرد صابون را بفهمیم.
عملکرد صابون
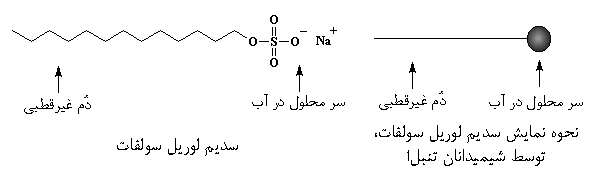
مولکولهای صابون از اختلال شخصیت چندگانه رنج میبرند، ولی شخصیت دوگانهی آنها همواره آشکار است. صابون، یا مادهی فعال سطحی، دو سر با حلالیتهای متفاوت دارد. یک انتهای آن که دم نامیده میشود، یک هیدروکربن طولانی است و در ترکیبات آلی غیر قطبی حل میشود و انتهای دیگر که سر نامیده میشود، اغلب نمکی از سدیم یا پتاسیم است که در آب محلول است. نمک محلول در آب میتواند نمک یک اسیدکربوکسیلیک یا یک اسیدسولفونیک باشد. واژه ی تخصصی مربوط به نمایش شیمیایی این «شخصیت دوگانه»، آمفیپاتیک یا دومحیطدوست میباشد.
تنها یک مولکول صابون کار زیادی انجام نمی دهد. اما زمانی که یک دسته از آنها را با هم در نظر بگیرید، اتفاق جالبی می افتد. در یک غلظت معین در آب، مولکول های صابون اجتماع می کنند و مایسل ها را تشکیل می دهند. این غلظت را غلظت بحرانی مایسل، یا به اختصار CMC می نامند. نکته ی مهم این است که در مایسل ها دم ها به طرف داخل هستند. 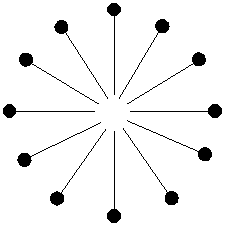
کثیفیها، چربیها و چرکهای روی دستان شما اغلب، آلی هستند و به این شباهت دارند:
![]()
وقتی شما دستهای خود را با آب محتوی صابون میشویید، ذرهی چرک، میان مایسلها میرود و در دُم آلی مایسل حل میشود.
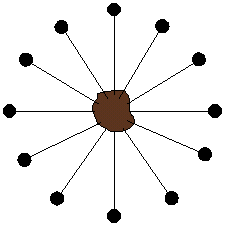
حالا چرک در مایسل حل شده است، و مایسل در آب حل شده است. بدین ترتیب با مقداری آب، میتوان چرک و کثیفی نامحلول در آب را از روی دست پاک کرد.
حال یک سوال برای شما: چرا حمام کردن در اقیانوس مشکل است؟
و سرانجام… پلیمریزاسیون امولسیونی
در یک پلیمریزاسیون امولسیونی، صابون یا ماده ی فعال سطحی، به میزانی در آب ریخته و حل می شود که غلظت بحرانی مایسل () به دست آید. داخل مایسل فضای لازم را برای پلیمریزاسیون فراهم می کند. یک مونومر (مانند استایرن یا متیل متاکریلات) و یک شروع کننده ی رادیکال آزاد محلول در آب به سیستم اضافه می گردد، و کل ظرف واکنش به هم زده می شود. پلیمریزاسیون های امولسیونی همیشه به صورت رادیکال آزاد انجام می شوند، زیرا انتهای زنجیر آنیونی یا کاتیونی، به سرعت به وسیله آب غیر فعال می گردند.
محصول یک پلیمریزاسیون امولسیونی، لاتکس نامیده میشود.
موقعیت مونومر
هنگامی که همهی مواد در ظرف ریخته شد، مونومر را میتوان در سه محل مختلف یافت. نخست، مونومر میتواند در قطرههای مونومری بزرگی باشد که در آب سرگردان اند. دوم، بخشی از مونومر میتواند در آب حل شود، که البته بسیار بعید است. (به یاد داشته باشید که مونومرهای آلی از قبیل استایرن و متیلمتاکریلات، آب گریز هستند.) و در نهایت، مونومر میتواند درون مایسلها وجود داشته باشد، و این دقیقاً همان جایی است که تمایل داریم. اکنون نگاهی به تعریف ابتدای این صفحه بیاندازید. مایع امتزاج ناپذیر، مونومر آب گریز است، مایع اصلی آب، و امولسیفایر همان صابون است.
شروع و پلیمریزاسیون
مرحلهی شروع، زمانی رخ میدهد که بخشی از شروعکننده به درون مایسل مهاجرت کند و با یک مولکول مونومر واکنش دهد. معمولاً از شروعکنندههای محلول در آب مانند پراکسیدها و پرسولفاتها استفاده میشود (این مواد از وقوع پلیمریزاسیون در قطرههای مونومری بزرگ نیز جلوگیری میکنند). وقتی پلیمریزاسیون شروع میشود، مایسل به صورت یک ذرهی پلیمری درمی آید. ذرات پلیمری میتوانند تا جرم مولکولیهای بسیار بالا رشد کنند، به خصوص اگر غلظت شروعکننده کم باشد، که باعث کم شدن غلظت رادیکال و سرعت اختتام هم میشود. به همین دلیل، بعضاً از یک عامل انتقال زنجیر هم استفاده میشود تا وزن مولکولی، خیلی بالا نرود.
رشد
مونومر از قطرههای مونومری بزرگ به مایسلها مهاجرت میکند تا پلیمریزاسیون ادامه یابد. به طور متوسط، به ازای هر مایسل یک رادیکال وجود دارد. از این رو، رقابت چندانی میان زنجیرهای در حال رشد در ذرات، برای مونومر وجود ندارد، بنابراین وزن مولکولی آنها نزدیک هم است و پراکندگی نزدیک به یک میباشد. عملاً در پلیمریزاسیونهای امولسیونی، همه ی مونومرها مصرف میشوند، و در نتیجه لاتکس تولید شده، بدون خالصسازی قابل استفاده است. این مسئله برای رنگها و پوششها از اهمیت خاصی برخوردار است. فقط کافی است مقداری رنگ به لاتکس اضافه شود و درون قوطی ریخته شود تا برای مصرف آماده گردد.
جنبهی قابل توجه پلیمریزاسیون امولسیونی در این است که میتوان آنچه در هر مایسل میگذرد را به عنوان یک پلیمریزاسیون تودهای کوچک در نظر گرفت؛ ولی بر خلاف پلیمریزاسیون تودهای متداول، هیچ مونومر واکنش ندادهای باقی نمیماند و هیچ «نقطه ی داغ» حرارتی به وجود نخواهد آمد. در پلیمریزاسیون تودهای (یعنی پلیمریزاسیون بدون حلال، و فقط با حضور مونومر و شروعکننده)، نقاط داغ حرارتی، باعث تخریب و رنگرفتگی میشوند، و انتقال زنجیر هم توزیع جرم مولکولی را پهن میکند. افزایش دما گاهی باعث میشود، سرعت واکنش بسیار بالا رود. اما در پلیمریزاسیون امولسیونی، آب به عنوان یک حمام حرارتی برای تمام آن رآکتورهای کوچک عمل میکند و مانع از انفجار آنها میگردد.
وزن مولکولی
این مطلب هم جالب است: سرعت پلیمریزاسیون با سرعت ناپدید شدن مونومرها برابر است. سرعت ناپدید شدن مونومرها با افزایش تعداد ذرات پلیمری، بیشتر میشود، و برای داشتن ذرات بیشتر باید مایسلهای بیشتری وجود داشته باشد. اگر صابون غلظت بیشتری داشته باشد، مایسلهای بیشتری نیز وجود خواهد داشت. حال فرض کنید که غلظت شروعکننده ثابت بماند. این حالت موجب ایجاد ذرات بیشتر، و رادیکالهای کمتر میشود، یعنی نسبت تعداد رادیکالها به مایسل کمتر از یک میشود. به عبارت دیگر، سرعت مرحله ی اختتام تا زمانی که غلظت رادیکالها کم است، پایین خواهد بود.
نتیجهی نهایی این است که کاهش غلظت شروعکننده، وزن مولکولی و سرعت پلیمریزاسیون را افزایش میدهد. این امر، کاملاً عکس پلیمریزاسیون تودهای و محلولی است. در این دو نوع پلیمریزاسیون، برای افزایش سرعت پلیمیزاسیون، باید دمای محیط واکنش، یا غلظت شروعکننده را افزایش داد، که هر دو عمل باعث افزایش سرعت اختتام، و کاهش وزن مولکولی خواهند شد.
کاربردها
ولی این روش پلیمریزاسیون چقدر کاربرد دارد؟ پلی(وینیل استات)، پلیکلروپرن، پلیمتاکریلاتها ، پلی(وینیل کلراید)، پلیآکریلآمید، و کوپلیمرهای پلیاستایرن، پلیبوتادیان، و پلیآکریلونیتریل در صنعت از طریق پلیمریزاسیون امولسیونی تولید میشوند.
در جدول زیر تمام مزایا و معایب سه نوع پلیمریزاسیون (تودهای، حلالی، امولسیونی) به صورتی ساده آورده شده است.
| فرآیند پلیمریزاسیون | مزایا | معایب |
| توده ای | فقط مونومر حضور دارد و مادهی اضافهای وجود ندارد، وزنهای مولکولی بالایی به دست میآید. | نقاط داغ حرارتی، ویسکوزیتهی بالا، حضور مونومر واکنش نداده |
| حلالی | کنترل دمای آسان، کنترل وزن مولکولی | حلال باید جدا شود، انتقال زنجیر به حلال |
| امولسیونی | تمام مونومرها واکنش می دهند، لاتکس به همان شکل قابل استفاده است، قابلیت کنترل حرارتی، می توان موادی با Tg پایین تولید کرد، ویسکوزیته ی پایین | وجود مواد فعال سطحی ممکن است موجب ایجاد حساسیت به آب گردد. |
مراجع و مطالعات بیشتر
(مطالعات پیچیده تر و مفصل تر)
- Odian, G., “Principles of Polymerization” 3rd Ed., John Wiley and Sons, Inc., New York, 1991.
- Rosen, S.L., “Fundamental Principles of Polymeric Materials” 2nd Ed., John Wiley and Sons, Inc., New York, 1993.
 my
my
سلام
اکثر مطالبتون به زبون ساده است .
اگه امکان داره طیف سنجی ir رو هم ساده تر توضیح بدین و هم چنین دستگاه های دیگه شناسایی از قبیل کروماتوگرافی گازی و طیف سنجی UV رو هم اضافه کنید .
ممنون از زحماتتون
سلام وقت بخیر چه موادی رو میتوان با استایرن مونومر اضافه کرد در صورتی که خواص استایرن مونومر تغییر چندانی نکند؟(متانول؟اتر؟تولوئن؟ و یا اینکه مواد دیگری اگر هست محبت کنید بفرمایید)
تشکر بابت زحماتتون
خیلی رسا و ب زبان ساده بود مرسی
ممنون از مطالب خوبتان